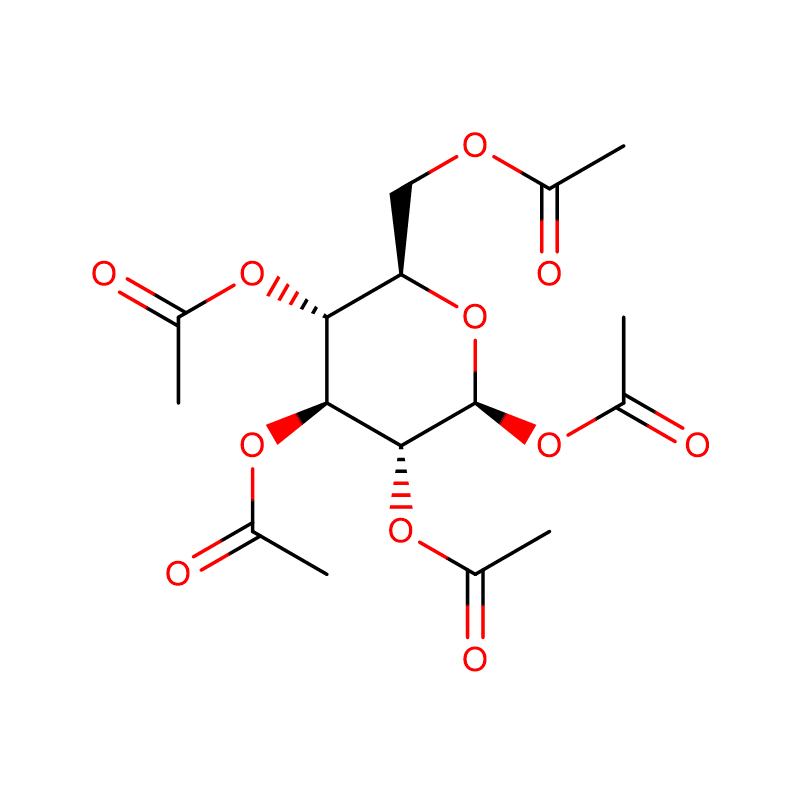
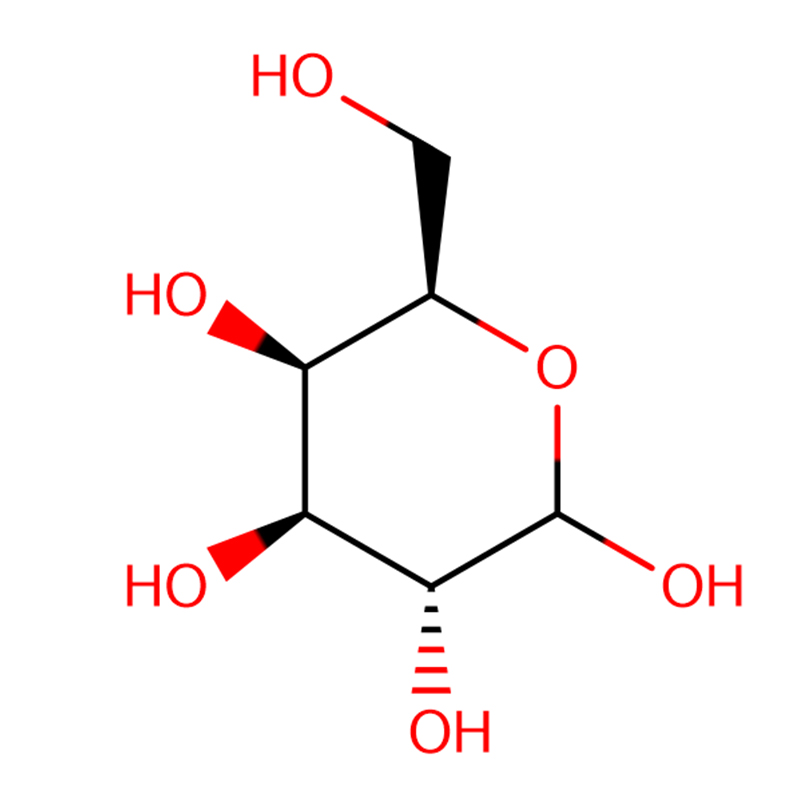
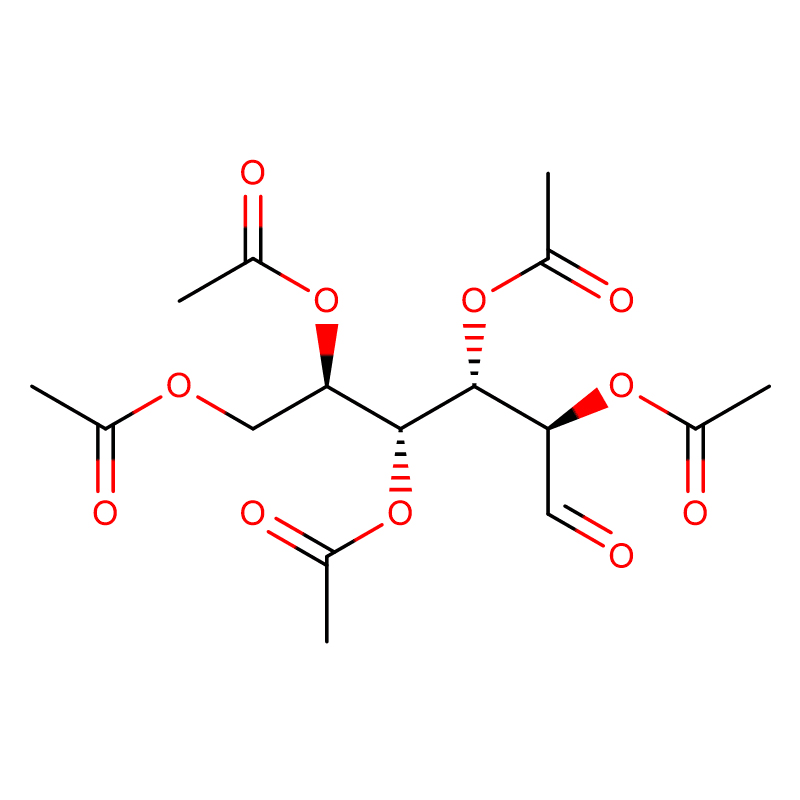
4-NITROPHENYL-ALPHA-D-MANNOPYRANOSIDE CAS:10357-27-4 Bột trắng nhạt 98%
| Số danh mục | XD90011 |
| tên sản phẩm | 4-Nitrophenyl-alpha-D-mannopyranoside |
| CAS | 10357-27-4 |
| Công thức phân tử | C12H15NO8 |
| trọng lượng phân tử | 30301,25 |
| Chi tiết lưu trữ | -2ĐẾN -8°C |
| Bộ luật thuế quan hài hòa | 29400000 |
Đặc điểm kỹ thuật sản phẩm
| Nước | <5% Karl Fische |
| độ hòa tan | 1% trong DMF rõ ràng và không màu |
| độ tinh khiết | 4-Nitrophenol tự do <200ppm |
| HPLC | >98% |
| Vẻ bề ngoài | Bột trắng |
Những hiểu biết cơ học về một họ alpha-mannosidase phụ thuộc vào Ca2 + trong cộng sinh đường ruột của con người.
Vi khuẩn ruột kết, được minh họa bởi Bacteroides thetaiotaomicron, đóng vai trò chính trong việc duy trì sức khỏe con người bằng cách khai thác các họ glycoside hydrolase (GH) lớn để khai thác polysacarit trong chế độ ăn uống và glycans chủ làm chất dinh dưỡng.Việc mở rộng họ GH như vậy được minh họa bằng 23 họ GH92 glycosidase được mã hóa bởi bộ gen B. thetaiotaomicron.Ở đây chúng tôi chỉ ra rằng đây là những alpha-mannosidase hoạt động thông qua một cơ chế dịch chuyển duy nhất để sử dụng N-glycans chủ.Cấu trúc ba chiều của hai mannosidase GH92 xác định một họ protein hai miền trong đó trung tâm xúc tác nằm ở giao diện miền, cung cấp hỗ trợ axit (glutamate) và bazơ (aspartate) để thủy phân trong Ca(2+)- cách phụ thuộc.Cấu trúc ba chiều của GH92 trong phức hợp với chất ức chế cung cấp cái nhìn sâu sắc về tính đặc hiệu, cơ chế và hành trình cấu tạo của xúc tác.Ca(2+) đóng vai trò xúc tác chính trong việc giúp làm biến dạng mannoside khỏi cấu trúc ghế (4)C(1) ở trạng thái cơ bản của nó để hướng tới trạng thái chuyển tiếp.(Tài liệu tham khảo: Nat.hóa học.sinh học.6, 125-32, (2010)
Sắc ký ái lực phía trước của ovalbumin glycoasparagines trên cột concanavalin A-sepharose.Một nghiên cứu định lượng về tính đặc hiệu liên kết của lectin.
Sự tương tác của concanavalin A (ConA) cố định Sepharose 4B với 10 glycoasparagin có nguồn gốc từ ovalbumin đã được nghiên cứu định lượng bằng sắc ký ái lực phía trước.Trong phương pháp này, dung dịch cacbohydrat được đưa liên tục vào cột ConA-Sepharose và độ trễ của mặt trước rửa giải được đo như một thông số về cường độ tương tác.Có thể xác định hằng số phân ly (Kd) cho mỗi sacarit với ConA.Một phân tích về sự gắn kết của p-nitrophenyl-alpha,D-mannoside đã chỉ ra rằng các đặc tính gắn kết của ConA về cơ bản không thay đổi sau khi cố định trên Sepharose 4B.Mỗi glycoasparagin ovalbumin được dán nhãn tritium bằng phương pháp methyl hóa khử để phân tích.So sánh các giá trị Kd thu được cho thấy rằng liên kết của ConA thay đổi đáng kể với sự khác biệt rất nhỏ về cấu trúc của chuỗi glycosyl.Kết quả cho thấy rằng ConA nhận ra cấu trúc chuỗi glycosyl cụ thể, Man alpha 1-6(Man alpha 1-3)Man, trong đó ít nhất một nhóm hydroxyl ở vị trí C-3 của mannose được liên kết với C-6 phải ở trạng thái tự do.